Autores:
Dres. Oriana Bastidas, Juan Carlos Díaz, Jorge Marín, Julián Aristizábal, Cesar Niño, Mauricio Duque
Texto:
Las Infecciones de dispositivos cardiacos electrónicos implantables afectan aproximadamente al 2% de todos los procedimientos de implantes y tienen un impacto importante tanto en la morbilidad de los pacientes como en los costos de la atención en salud. [1] Existen procedimientos que implican un mayor riesgo tales como cambio de generador, actualización de dispositivo, o revisión de electrodo/bolsillo, ya que se ha reportado que hasta el 60% de las infecciones de bolsillo están relacionados con la manipulación previa del dispositivo. [2, 3] Las estrategias descritas para reducir las infecciones son la preparación preoperatoria de la piel con clorhexidina, el uso de antibiótico profiláctico y el uso de una envoltura antibacteriana bioabsorbible. No obstante, a pesar de las mejores prácticas se encuentra contaminación bacteriana de la cápsula en el 33% de los pacientes, de estos el 7% desarrolla posteriormente infección de bolsillo y en un tercio de estos casos, el agente causal se identifica como resistente a la meticilina, por lo anterior la implementación de intervenciones destinadas a reducir la carga bacteriana dentro de la cápsula son de gran importancia.[4] Se ha propuesto la capsulotomía profiláctica para reducir la tasa de infecciones, sin embargo, es un procedimiento cruento que se asocia a aumento en la tasa de hematomas y no se asocia a una reducción significativa de las infecciones relacionadas a dispositivos. Recientemente se ha promocionado el uso de una envoltura antibacteriana para reducir el riesgo de infección en pacientes de alto riesgo, sin embargo, esta se asocia a mayores costos al sistema de salud y no está disponible en todos los países. [5]
El gluconato de clorhexidina (GCH) es un fármaco con actividad bacteriostática, bactericida contra hongos, bacterias gram positivas y gram negativas, tiene casi el 100% de eficacia antiséptica en 30 segundos de aplicación y actividad prolongada debido a su capacidad de unirse al tejido (hasta 48 horas), que no se afecta por sangre u otros fluidos corporales. [6] El GCH tradicionalmente se ha utilizado para la preparación de la piel para prevenir infecciones del sitio quirúrgico en todo tipo de cirugías. Adicionalmente, se ha descrito para la irrigación de heridas en pacientes sometidos a artroplastia total de rodilla y cadera, aumento o reconstrucción mamaria, cierre de ileostomía y parto por cesárea como estrategia para reducir las infecciones.[7-9] Su uso en el lavado del bolsillo para la prevención de infecciones asociadas al uso de dispositivos de estimulación cardíaca (CIED) no había sido descrito. Recientemente, publicamos nuestra experiencia en la que se buscó evaluar la seguridad y potencial eficacia del lavado de bolsillo con GCH vs irrigación con solución salina normal (NS) para la prevención de infecciones por CIED.
Se evaluaron de forma prospectiva 1405 pacientes que fueron llevados a procedimientos, de alto riesgo definidos como aquellos que implican la apertura de un bolsillo preexistente (cambio de generador, actualización del dispositivo o revisión de electrodos/bolsillo)
El lavado se realizó de la siguiente manera: usando solución de GCH al 2% sin alcohol se frota manualmente por fuera y dentro del bolsillo durante al menos 1 minuto, posteriormente se realiza lavado con 500 o 1000 cc de NS hasta que no queden residuos para evitar irritación en la piel o de los tejidos, se seca con apósitos estériles el bolsillo y la herida, luego se cierra la herida con sutura absorbible de forma continua.
Evidenciamos una incidencia significativamente menor en el desenlace primario definido como cualquier infección asociada al dispositivo después de un año del procedimiento, el resultado se observó en el grupo GCH (0,4% frente a 2,3% del grupo de solución salina; Cox proporcional [HR] 0,205; IC del 95% 0,07– 0,63; P 0.005). Sobre el análisis multivariado el uso de GCH se asoció con un menor riesgo de infección (Cox proporcional HR 0,16; IC del 95%: 0,05 a 0,52; P 0.002). Esta diferencia en el riesgo fue impulsada por una reducción significativa en el riesgo de infección no sistémica, incluida infección de bolsillo, extrusión de electrodos, o deformidad del bolsillo con riesgo de extrusión (0,3% vs 2%; P = 0,002). No se evidenciaron eventos adversos con uso de GCH.
Durante el seguimiento a largo plazo (mediana de seguimiento 672 [303–1373] días; 406 [204–734] días en el grupo GCH frente a 1.568 [907–2108] días en el grupo NS; P < 0,001) la infección ocurrió con menos frecuencia en el grupo GCH (0,7% frente a 3,3%, respectivamente; FC proporcional de Cox 0,4; IC del 95%: 0,16 a 0,98; P 0.044).
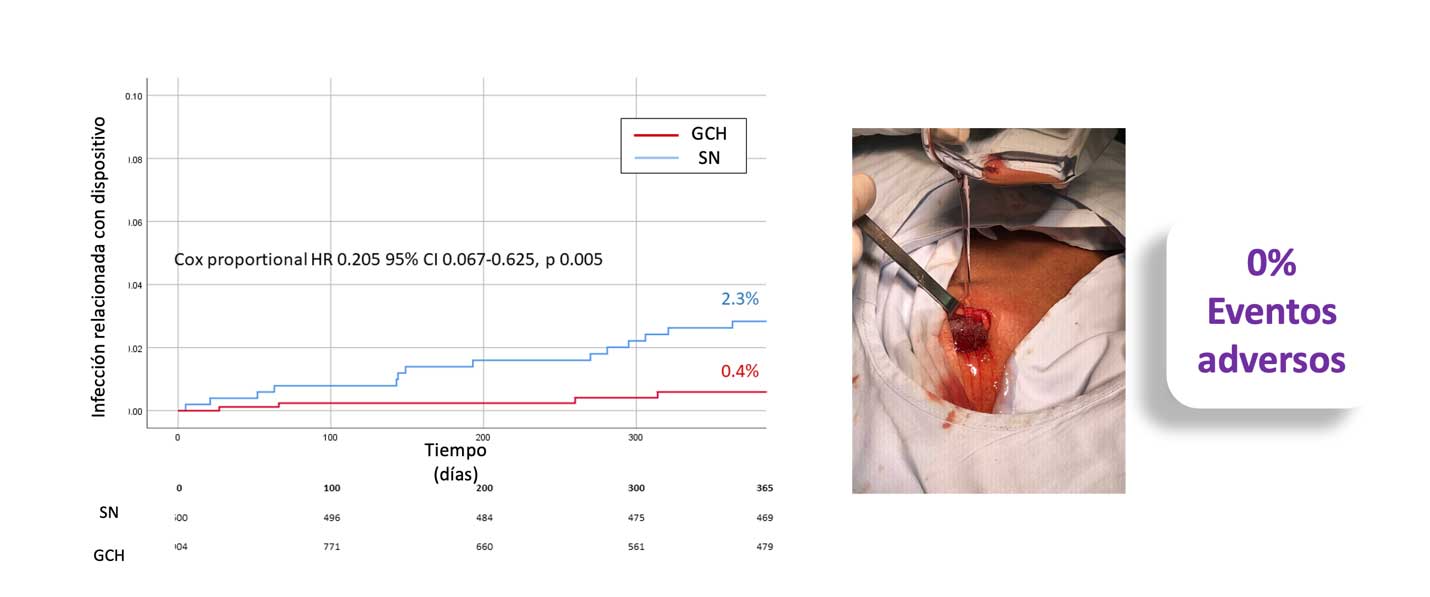
Por todo lo anterior en nuestra experiencia, el uso del lavado de bolsillo con GCH en pacientes sometidos a procedimientos de alto riesgo se asocia a una reducción significativa en el riesgo de infección y dado el bajo costo del GCH, su amplia disponibilidad, la falta de efectos adversos podría considerarse como estrategia para reducir las infecciones relacionadas con el uso de dispositivos.
.
1. Lakshmanadoss, U., et al., Incidence of Pocket Infection Postcardiac Device Implantation Using Antibiotic versus Saline Solution for Pocket Irrigation. Pacing Clin Electrophysiol, 2016. 39(9): p. 978-84.
2. Arana-Rueda, E., et al., Repeated procedures at the generator pocket are a determinant of implantable cardioverter-defibrillator infection. Clin Cardiol, 2017. 40(10): p. 892-898.
3. Esquer Garrigos, Z., et al., Diagnostic evaluation and management of culture-negative cardiovascular implantable electronic device infections. Pacing Clin Electrophysiol, 2018.
4. de Oliveira, J.C., et al., Efficacy of antibiotic prophylaxis before the implantation of pacemakers and cardioverter-defibrillators: results of a large, prospective, randomized, double-blinded, placebo-controlled trial. Circ Arrhythm Electrophysiol, 2009. 2(1): p. 29-34.
5. Tarakji, K.G., et al., Antibacterial Envelope to Prevent Cardiac Implantable Device Infection. N Engl J Med, 2019. 380(20): p. 1895-1905.
6. Schmidt, K., et al., Chlorhexidine Antiseptic Irrigation Eradicates Staphylococcus epidermidis From Biofilm: An In Vitro Study. Clin Orthop Relat Res, 2018. 476(3): p. 648-653.
7. Darouiche, R.O., et al., Chlorhexidine-Alcohol versus Povidone-Iodine for Surgical-Site Antisepsis. N Engl J Med, 2010. 362(1): p. 18-26.
8. Luwang, A.L., et al., Chlorhexidine-alcohol versus povidone-iodine as preoperative skin antisepsis for prevention of surgical site infection in cesarean delivery-a pilot randomized control trial. Trials, 2021. 22(1): p. 540.
9. Goztok, M., et al., Does Wound Irrigation with Clorhexidine Gluconate Reduce the Surgical Site Infection Rate in Closure of Temporary Loop Ileostomy? A Prospective Clinical Study. Surg Infect (Larchmt), 2018. 19(6): p. 634-639.